
 Flash News
Flash News
Fuste dr*gë dhe sende të paligjshme në qeli, arrestohet polici i burgut të Drenovës
Lavrov: NATO po rrezikon vetëshkatërrimin me buxhetin e ri ushtarak
Kurti e Vuçiç "përballen" nesër në Shkup
Bie nga skelat, humb jetën punëtori i ndërtimit në Berat
Prokuroria dërgon për gjykim dy zyrtarët e Bashkisë Korçë
FDA miraton "alpelisib" për gratë me kancer gjiri të avancuar, ndikon drejtpërdrejtë në mbijetesën e tyre
Administrata amerikane e ushqimit dhe drogës (FDA) ka aprovuar alpelisib (Piqray, më parë BYL719), një inhibitor kinase i zhvilluar nga Novartis, në kombinim me fulvestrant (Faslodex? AstraZeneca), për trajtimin e grave postmenopauzale dhe burra me hormon (HR + / HER2-) dhe një gjen i katalizuar alfanik (fosfatidilinozitol-3-kinaza) alfa (PIK3CA), kancer i gjirit i avancuar ose metastatik, i zbuluar nga një test i aprovuar nga FDA pas progresionit në ose pas një regjimi endokrin.
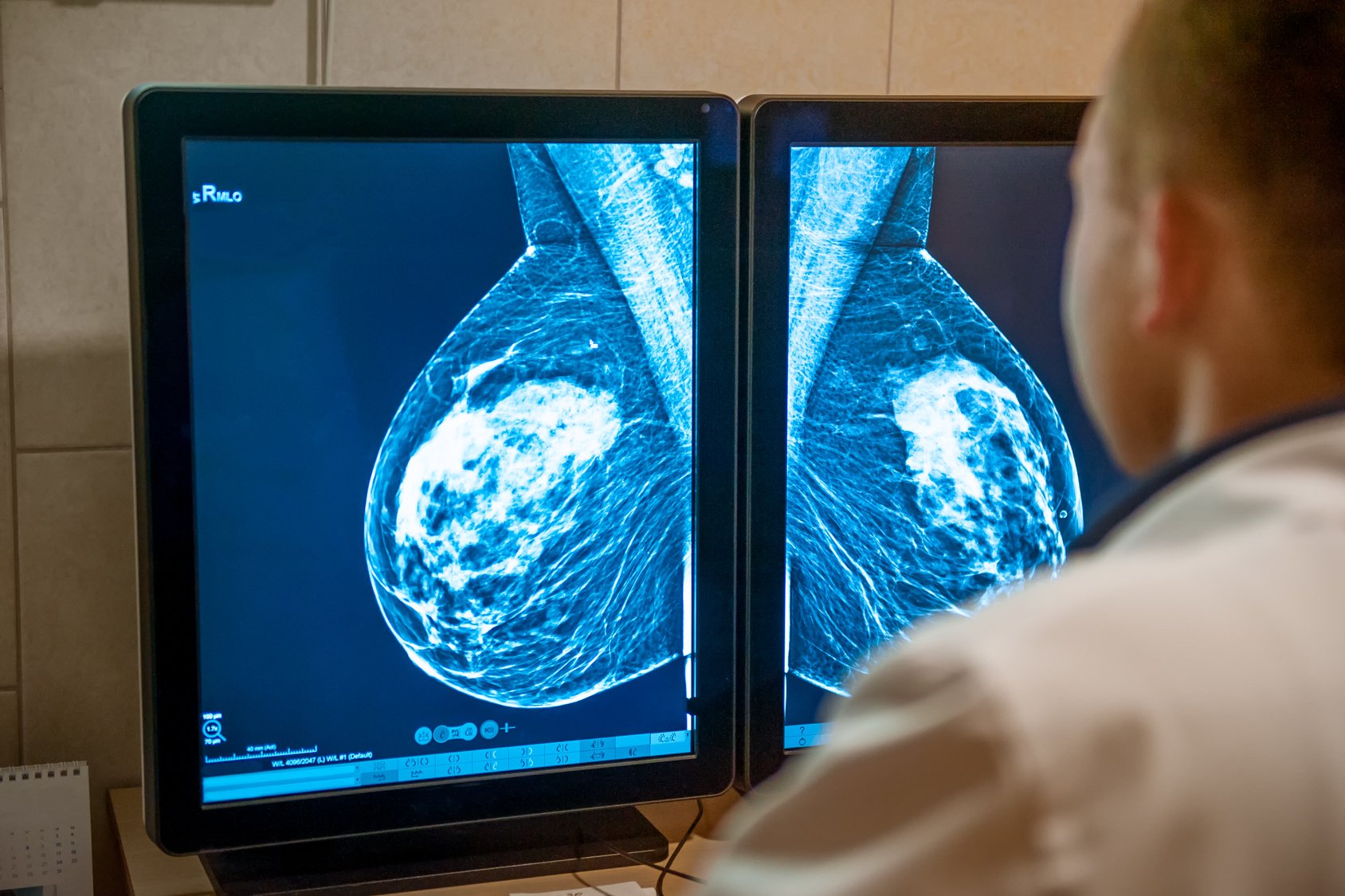
PIK3CA është gjeni më i zakonshëm i ndryshuar në HR + / HER2 - kanceri i gjirit. Përafërsisht 40% e pacientëve që jetojnë me HR + / HER2 - kanceri i gjirit kanë këtë mutacion. Mutacionet PIK3CA shoqërohen me rritjen e tumorit, rezistencën ndaj trajtimit endokrin dhe një prognozë të dobët të përgjithshme. Alpelisib synon efektin e mutacioneve PIK3CA dhe mund të ndihmojë në kapërcimin e rezistencës endokrine në kancerin e gjirit të avancuar të HR +.
Në 24 maj të 2019-ës, FDA (Food and Drug Administration) ka aprovuar alpelisib (PIQRAY, Kompania Farmaceutike Novartis) në kombinim me fulvestrant për gratë postmenopauzale (pas menopauzës) dhe burrat me hormon receptor (HR)-pozitiv.
Alpelisib është një inhibitor oral i phosphatidylinositol 3-kinase (PI3K). Ky ilaç pengon rritjen e qelizave tumorale dhe ndikon në mënyrë të drejtpërdrejtë në mbijetesën e të prekurve me kancer gjiri të avancuar. Sinjalizimi i rregulluar PI3K mund të kontribuojë në rezistencën e tumorit ndaj një sërë agjentësh antineoplastikë.
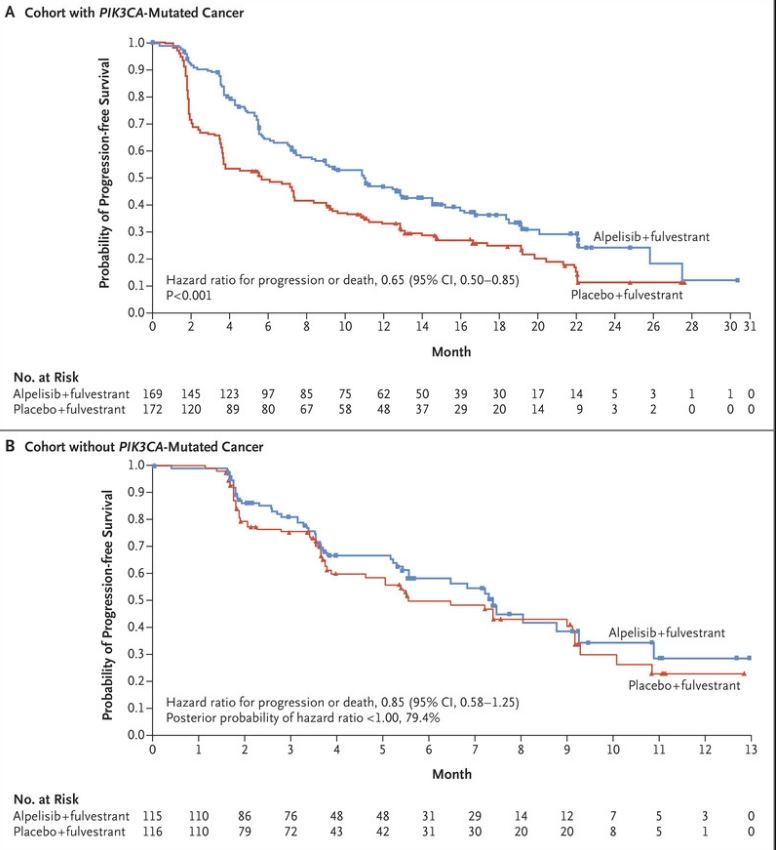
Aprovimi i FDA-së u bazua në rezultatet e fazës së tretë të studimit SOLAR 1 (NCT02437318), një studim që përfshinte 572 pacientë, gra postmenopauzale dhe burra, me HR-pozitive, HER2-negative, me kancer gjiri të avancuar ose metastatik, të cilëve sëmundja u ka përparuar gjatë apo pas marrjes së një inhibitori aromatase. Ky studim tregoi se alpelisib plus fulvestrant pothuajse dyfishon mbijetesën mesatare pa progres (PFS) në krahasim me fulvestrant vetëm në HR + / HER2 - pacientët e kancerit të gjirit të avancuar me një mutacion PIK3CA (median PFS 11.0 muaj vs 5.7 muaj, HR = 0.65, 95% CI: 0.50-0.85, p <0.001) [2]
Efektet më të zakonshme anësore, duke përfshirë anomalitë laboratorike në përdorimin e alpelisib plus fulvestrant ishin: rritja e glukozës, , diarreja, skuqja, ulja e numrit të limfociteve, rritja e transferimit të glutamilit gama, lodhje, ulja e hemoglobinës, vjellje, uljes të peshës, ulje të kalciumit, zvogëlimi i glukozës.
Doza e rekomanduar alpelisib është 300 mg (dy tableta 150 mg) duke i marrë në formë orale (nga goja) dy herë bë ditë. Kur jepet me alpelisib, dozë e rekomanduar e fulvestrant është 500 mg e administruar në formë intramuskulare në ditët 1, 15 dhe 29 dhe një herë në muaj më pas.
"Ne jemi krenar të ofrojmë një mundësi të re trajtimi që trajton në mënyrë specifike nevojat e pacientëve që jetojnë me këtë mutacion," - tha Susanne Schaffert, PhD, CEO, Novartis Oncology.
Artikulli i plotë: U.S FOOD & DRUG ADMINISTRATION
Të fundit


Replikat Rama-Farage, Bushati: Këshillat e një politikani shqiptar s’i hyjnë në punë Anglisë
30 Qershor 2025, 22:39
Seanca e dytë për ligjin e zonave të mbrojtura, Zhupa: Antikushtetues dhe i rrezikshëm
30 Qershor 2025, 22:18
Gjyqi për 'Partizanin', ish-prokurori: 90% e seancave dështojnë për mos njoftim
30 Qershor 2025, 21:56
E përjashtuan nga Policia/ Efektivi i infiltruar: Alkool s’kam pirë, veç drogë nga puna
30 Qershor 2025, 21:53

Konflikti Izrael-Iran, Bushati: Shqiptarët duhet të jenë të shqetësuar
30 Qershor 2025, 21:32
Rrahën për vdekje të burgosurin në Burgun e Reçit, prokuroria merr të pandehur 6 gardianë!
30 Qershor 2025, 21:15
Fuga: Gazetaria në Shqipëri sot në krizë të fortë
30 Qershor 2025, 21:07
"Nuk ka vend për panik"/ Moore: Serbia nuk guxon të sulmojë Kosovën!
30 Qershor 2025, 20:49
Fuste dr*gë dhe sende të paligjshme në qeli, arrestohet polici i burgut të Drenovës
30 Qershor 2025, 20:35
Temperaturat mbi 40 gradë, Franca mbyll centralet bërthamore dhe shkollat
30 Qershor 2025, 20:28
Lavrov: NATO po rrezikon vetëshkatërrimin me buxhetin e ri ushtarak
30 Qershor 2025, 20:13
Turqia kundër “shtetit bektashi” në Shqipëri: Hiqni dorë nga kjo ide!
30 Qershor 2025, 20:03

I akuzuar për abuzim sek*ual, producenti Diddy pret sot vendimin e gjykatës
30 Qershor 2025, 19:40


"Gjyqi për dosjen Partizani i paqartë"/ Gjokutaj: Ka ndikim politik në drejtësi!
30 Qershor 2025, 19:00
Kurti e Vuçiç "përballen" nesër në Shkup
30 Qershor 2025, 18:44
Turizmi: sezon i ri, probleme të vjetra
30 Qershor 2025, 18:27
Matura Shtetërore/ Publikohen notat e provimeve të lëndës me zgjedhje, 360 maturantë ngelës
30 Qershor 2025, 18:16
Thashetheme dhe tensione me kolegët, 3 shenjat më pa fat për javën e parë të Korrikut
30 Qershor 2025, 18:10
Bie nga skelat, humb jetën punëtori i ndërtimit në Berat
30 Qershor 2025, 17:51

"Non-grata e Berishës duhet të rishikohet"/ Ish-zyrtari i lartë i SHBA: U ndëshkua pa prova!
30 Qershor 2025, 17:23

Pas murtajës një tjetër sëmundje shfaqet te bagëtitë, izolohen dy familje në Dibër
30 Qershor 2025, 16:50
Strehim gati falas: Lindja gjermane kundër shpopullimit
30 Qershor 2025, 16:43

Hamasi thotë se gati 60 persona janë vrarë në Gaza, ndërsa Trump bën thirrje për armëpushim
30 Qershor 2025, 16:14
Mbytjet tragjike në plazhe/ Eksperti Softa: Neglizhencë dhe paaftësi nga institucionet!
30 Qershor 2025, 16:00
Në 6 muaj 1260 denoncime për dhunë në familje, çdo ditë rrihen 7 gra ose burra
30 Qershor 2025, 15:57
ChatGPT ul punësimet e të rinjve, ja sektorët më të prekur në botë
30 Qershor 2025, 15:44
Portet europiane mbingarkohen për shkak të tarifave të Trump-it
30 Qershor 2025, 15:30
Prokuroria dërgon për gjykim dy zyrtarët e Bashkisë Korçë
30 Qershor 2025, 15:19
"Arrestimi im është politik"/ Meta: SPAK vegël e qeverisë! Demokracia shqiptare në rrezik
30 Qershor 2025, 15:07
Lezhë/ Policia vendos 3165 masa administrative, pranga 19 drejtuesve të mjeteve
30 Qershor 2025, 14:55
Të rinjtë lënë Shqipërinë në kërkim të një të ardhmeje më të qëndrueshme
30 Qershor 2025, 14:47
Verë me nxehtësi rekord, kërcënimet për shëndetin dhe masat parandaluese
30 Qershor 2025, 14:36

Blushi: Dënojmë procesin politik gjyqësor ndaj Berishës, farsë e turpshme
30 Qershor 2025, 14:20
Konstituimi i Kuvendit, Osmani fton në takim krerët politikë
30 Qershor 2025, 14:07

Vala e të nxehtit ‘pushton’ Evropën, Spanja regjistron temperatura deri në 46 gradë Celsius
30 Qershor 2025, 13:42
Aksident në Vlorë, makina merr përpara 2 turistë
30 Qershor 2025, 13:32

Kurti konfirmon pjesëmarrjen në darkën e sotme zyrtare në Shkup
30 Qershor 2025, 13:03

Sherr mes 4 të miturve në Kosovë, njëri prej tyre plagoset me thikë
30 Qershor 2025, 12:38
Rinumërimi/ Korreshi: Në Fier u bë masakër elektorale me patronazhistë dhe lekët e shtetit
30 Qershor 2025, 12:27
Raporti: Vajzat adoleshente, më të vetmuarat në botë
30 Qershor 2025, 12:20
Komisionarja Kos dhe udhëheqësit e Ballkanit takohen në Shkup për Planin e Rritjes
30 Qershor 2025, 12:07
Në kërkim nga Italia, kapet në Fier anëtari i një organizate kriminale
30 Qershor 2025, 11:55
Qindra familje të zhvendosura nga vala e sulmeve ajrore izraelite në Gaza
30 Qershor 2025, 11:45

Zenel Beshi: Krimineli që as 50 dënime nuk e lëvizin nga Britania
30 Qershor 2025, 11:23
Një variant i ri i Covid do të qarkullojë gjatë verës, ja simptomat
30 Qershor 2025, 11:14

Sot nis rinumërimi i 587 kutive të Fierit, a do ta mbajë mandati Zegjineja?
30 Qershor 2025, 10:50
Dosja “Partizani”, shtyhet më 21 korrik seanca në Gjykatën e Posaçme
30 Qershor 2025, 10:41
Dëshira e pakontrolluar për të vjedhur, çfarë është kleptomania, pse shkaktohet
30 Qershor 2025, 10:30
Kërkoi ndryshimin e masës së sigurisë, shtyhet më 7 korrik seanca për Malltezin
30 Qershor 2025, 10:24


Prodhimi për orë pune në Shqipëri 35% më i ulët se mesatarja rajonale
30 Qershor 2025, 09:54

Minimatura/ Provimi i fundit, rreth 28 mijë nxënës testohen sot në Gjuhën e Huaj
30 Qershor 2025, 09:40
Nis sot procesi gjyqësor për dosjen “Partizani”
30 Qershor 2025, 09:27
22 vatra zjarri në 24 orët e fundit në vend, 2 ende aktive
30 Qershor 2025, 09:21
Si kontrollohen mediat? Rasti 'Rama' dhe propaganda qeveritare
30 Qershor 2025, 09:13
Kryediplomati gjerman: Putin dëshiron kapitullimin e Ukrainës
30 Qershor 2025, 09:00
Këmbimi valutor, me sa shiten dhe blihen monedhat e huaja sot
30 Qershor 2025, 08:44
Grafiku/ Bie ndjeshëm rreziku sovran për Shqipërinë nga tregjet ndërkombëtare
30 Qershor 2025, 08:26
Horoskopi, çfarë kanë rezervuar yjet për ju
30 Qershor 2025, 08:11
Mot i kthjellët dhe vranësira kalimtare, ja parashikimi për këtë të hënë
30 Qershor 2025, 07:59
Posta e mëngjesit/ Me 2 rreshta: Çfarë pati rëndësi dje në Shqipëri
30 Qershor 2025, 07:47
Milani zyrtarizon dy largime në sulm
29 Qershor 2025, 21:57
6 rekordet tona
29 Qershor 2025, 21:30
Rrëzohet nga ballkoni 4-vjeçarja në Lezhë, dërgohet me urgjencë te Trauma
29 Qershor 2025, 21:09

"Vrau një grup të mirë politikanësh", Bregu: Basha na përzuri me një të rënë të lapsit
29 Qershor 2025, 20:07
Sekuestrohen pasuri me vlerë 12 milionë euro nga organizata e trafikut të kokainës
29 Qershor 2025, 19:39
Zjarri në Durrës, Blushi: Shteti ekziston vetëm në letra
29 Qershor 2025, 19:17

Zjarri rrezikon banesat në Vlorë, nis ndërhyrja me helikopter
29 Qershor 2025, 18:27
Franca zbaton ndalimin e pirjes së duhanit në plazhe dhe parqe
29 Qershor 2025, 18:02
Mundi Gjermaninë, Anglia U-21 shpallet kampione e Europës
29 Qershor 2025, 17:42
Trump kritikon prokurorët e Izraelit për gjyqin e Netanyahut i akuzuar për korrupsion
29 Qershor 2025, 17:08
Përfshihet nga flakët tregu ambulant në Durrës
29 Qershor 2025, 16:52
Zjarr masiv në fshatin Hoshtimë në Vlorë, flakët favorizohen nga era e fortë
29 Qershor 2025, 16:33

Ra nga humnera teksa ngjitej në mal, humb jetën shqiptari në Itali
29 Qershor 2025, 15:52

Tjetër aksident me monopatinë në Tiranë, makina përplas një 17-vjeçar
29 Qershor 2025, 15:07
Po lahej në det, humb jetën pushuesi në Durrës
29 Qershor 2025, 14:54
I dënuar me burg përjetë, gjendet celular në qelinë e Laert Haxhiut
29 Qershor 2025, 14:26
77 persona të ndaluar në protestë, Vuçiç paralajmëron arrestime të reja
29 Qershor 2025, 14:07
Përplasi tre të miturit me monopatinë në Tiranë, shoferi lihet në “arrest në shtëpi”
29 Qershor 2025, 13:51
